
Rasa ingin tahu dan keinginan untuk selalu mendapatkan yang terbaik dalam memecahkan semua masalah dalam kehidupan mengharuskan manusia untuk dapat mengembangkan imajinasinya serta mewujudkanyya. Adanya keinginan untuk menghasilkan suatu makhluk hidup yang memiliki perpaduan seluruh sifat positif dari makhluk hidup yang sudah ada menyebabkan manusia terus berusaha mengembangkan IPTEK. Hal ini dapat diwujudkan setelah ditemukannya ilmu genetika dan rekayasa genetika.Rekayasa genetika adalah gambaran dari bioteknologi yang di dalamnya meliputi manipulasi gen, kloning gen, DNA rekombinan, teknologi modifikasi genetik, dan genetika modern dengan menggunakan prosedur identifikasi, replikasi, modifikasi dan transfer materi genetik dari sel, jaringan, maupun organ (Karp, 2002; Nicholl, 2002). Sebagian besar teknik yang dilakukan adalah memanipulasi langsung DNA dengan orientasi pada ekspresi gen tertentu. Dalam skala yang lebih luas, rekayasa genetika melibatkan penanda atau marker yang sering disebut sebagai Marker-Assisted Selection (MAS) yang bertujuan meningkatkan efisiensi suatu organisme berdasarkan informasi fenotipnya (Lewin, 1999; Klug dan Cummings, 2002).
Dalam arti yang paling luas, rekayasa genetika adalah penerapan genetika untuk kepentingan manusia. Obyek rekayasa genetika mencakup hampir semua golongan organisme, mulai dari bakteri, fungi, hewan tingkat rendah, hewan tingkat tinggi, hingga tumbuh-tumbuhan. Pada hewan, rekayasa genetika sudah banyak dilakukan dengan berbagai tujuan yang bermanfaat bagi kehidupan manusia. Salah satu perkembangan terbaru dari rekayasa genetika pada hewan yang sangat digemari adalah ikan yang bisa bercahaya atau berpendar (terkenal dengan sebutan GloFish).
Penemuan GloFish
Perkembangan ilmu rekayasa genetika di berbagai bidang kehidupan menyebabkan terciptanya produk-produk baru hasil rekayasa genetika. Pada tahun 1999, Dr Zhiyuan Gong dan rekan-rekannya di National University of Singapore bekerja dengan gen yang mengkodekan Green Fluorescent Protein (GFP) atau protein hijau berpendar yang awalnya diekstraksi dari ubur-ubur. Mereka memasukkan gen tersebut ke dalam embrio ikan zebra (zebra danio, Danio rerio) yang memungkinkan untuk diintegrasi ke dalam genom ikan zebra.
Setelah diuji, ternyata ikan zebra yang telah disisipi gen ubur-ubur tadi menjadi berpendar terang di bawah cahaya putih alami dan sinar ultraviolet. Ikan zebra yang bisa berpendar inilah yang disebut dengan glowfish (ikan bercahaya).
Gambar 1. Ikan Zebra (sumber:
Penemuan ikan zebra yang bisa berpendar hijau ini adalah langkah awal dalam proses ini. Selanjutnya, National University of Singapore (NUS) mengajukan permohonan paten pada pekerjaan ini sehingga tak lama kemudian didapatkan ikan zebra yang tidak hanya berpendar hijau namun juga berpendar merah dari penambahan gen karang laut, dan oranye-kuning dengan penambahan varian gen ubur-ubur.
Setelah ditemukannya banyak variasi warna dari ikan yang bisa berpendar, para ilmuwan dari NUS, pengusaha Alan Blake dan Richard Crockett dari Yorktown Technologies, sebuah perusahaan di Austin-Texas, bertemu dan menyepakati ditandatangani dimana Yorktown memperoleh hak di seluruh dunia untuk memasarkan ikan zebra yang bisa berpendar. Ikan zebra ini kemudian dipatenkan dengan nama GloFish.
Tujuan dan Manfaat GloFish
Pada mulanya GloFish dibuat untuk digunakan sebagai indikator polusi. Para peneliti memasukkan gen pemicu yang akan mengaktifkan pancaran cahaya (dari gen ubur-ubur) pada ikan zebra sehingga apabila ikan zebra ini berada dalam lingkungan yang mengandung zat tertentu yang
berbahaya bagi lingkungan. Namun, seiring dengan berjalannya penelitian dan ditemukannya berbagai warna, sampai saat ini, modifikasi gen yang dilakukan terhadap jenis ikan zebra tersebut telah mendapatkan lima warna berbeda (Starfire Red®, Sunburst Orange®, Electric Green®, Cosmic Blue™ and Galactic Purple™) yang akan bersinar ketika berada di bawah sinar yang redup, maka produk ikan zebra yang bisa berpendar ini telah dipatenkan untuk dijual sebagai ikan hias/ikan aquarium.
GloFish terus berhasil dipasarkan di seluruh Amerika Serikat. Sejak diperkenalkan pada akhir tahun 2003, belum ada laporan dari setiap masalah ekologi terkait dengan penjualan mereka. Bahkan saat ini sedang terkenal di restoran-restoran makanan Jepang di Amerika pembuatan sushi glow in the dark (dikenal juga dengan glowing sushi) yaitu sushi yang dibuat dengan menggunakan daging GloFish.

Gambar 3. Glowing Sushi (sumber: www.glowingsushi.com)
Pembuatan GloFish
Ikan Zebra (Zebrafish)
Zebrafish (Danio rerio) adalah salah satu jenis ikan air tawar yang kecil (panjang 3 ± 4 cm). Meskipun rincian distribusinya tidak jelas, ikan zebra dapat tersebar luas di perairan dangkal, lambat mengalir di anak benua India. Mereka paling sering ditemui di kolam dangkal yang terhubung ke budidaya padi. (Spence et al, 2008 dan referensi di dalamnya). Ikan zebra ini merupakan salah satu spesies yang dapat dengan mudah disimpan dan dibesarkan di laboratorium sehingga biasa digunakan sebagai ikan peliharaan di akuarium.
Ikan zebra telah digunakan sebagai model organisme untuk mempelajari gen yang mengontrol perkembangan selama sekitar tiga puluh tahun. Ikan zebra dipilih sebagai sistem model genetik karena berbagai alasan.
1) Tubuhnya berukuran kecil sehingga bisa didapatkan banyak strain genetik dalam ruang kecil.
2) Mampu menghasilkan banyak keturunan dalam sekali reproduksi. Seekor betina ikan zebra dapat menghasilkan 100-200 telur dalam sekali reproduksi, dan mereka bertelur sekitar sekali seminggu. Telur-telur yang dihasilkan ini mampu berkembang dengan cepat dan mencapai kematangan seksual dalam 2-3 bulan.
3) Ikan zebra merupakan vertebrata, sehingga kontrol dari perkembangan genetik dan penyakit genetiknya mirip dengan manusia.
4) Ikan zebra jauh lebih murah daripada tikus, yang merupakan organisme vertebrata juga.
5) Embrio dari ikan zebra tembus cahaya, sehingga mudah untuk mengidentifikasi adanya mutan dengan perkembangan abnormal (Samantha Lindeman and Jennifer Liang)

Aequorea victoria
Aequorea victoria, juga kadang-kadang disebut ubur-ubur kristal, adalah salah satu jenid ubur-ubur hidrozoan bioluminescent atau hidromedusa yang ditemukan di lepas pantai barat Amerika Utara. Klasifikasi dari Aequorea victoria adalah sebagai berikut.
Kingdom: Animalia
Family: Aequoreidae
Phylum: Cnidaria
Genus: Aequorea
Class: Hydrozoa
Species: A. victoria
Aequorea victoria transparan dan berbentuk paying bulat atau bel. Ubur-ubur ini berdiameter sekitar 8-25 cm dan hanya hidup sekitar 6 bulan. Ubur-ubur transparan ini memiliki mulut yang sangat kontraktil dan manubrium di pusat hingga 100 kanal radial. Ubur-ubur ini biasanya memakan organisme bertubuh lunak.
Aequorea victoria memiliki sejarah hidup dimorfik, bergantian antara bentuk polip aseksual dan medusa bentuk planktonik seksual dalam pola musiman. Medusanya menghabiskan tahap pertama kehidupan berkembang dengan cepat, dan setelah mencapai kira-kira 3cm akan mulai memproduksi gamet untuk reproduksi.
Ubur-ubur ini mampu menghasilkan kilatan cahaya biru dengan melepaskan ion kalsium (Ca2+) yang berinteraksi dengan aequorin photoprotein. Cahaya biru yang dihasilkan pada gilirannya akan berubah menjadi hijau dengan sekarang terkenal green fluorescent protein (GFP). Aequorin dan GFP adalah alat penting yang digunakan dalam penelitian biologi. Pada tahun 1961, Shimomura dan Johnson mengisolasi aequorin protein dan yang kofaktor molekul kecil, coelenterazine, dari sejumlah besar ubur-ubur Aequorea victoria di Friday Harbor Laboratories. Penelitian ini juga menandai awal dari penelitian protein fluorescent hijau yang dirangkum oleh Shimomura. Untuk penelitian ke GFP, Osamu Shimomura dianugerahi Hadiah Nobel 2008 untuk bidang kimia , bersama dengan Martin Chalfie dan Roger Tsien.
Green Flourescent Protein (GFP)
The green fluorescent protein (GFP) adalah protein yang terdiri dari 238 residu asam amino (26,9 kDa) yang menunjukkan fluoresensi hijau terang bila terkena cahaya biru di rentang ultraviolet. Meskipun setelah berbagai penelitian ditemukan bahwa GFP tidak hanya ditemukan pada ubur-ubur A. Victoria, namun GFP tradisional mengacu pada protein pertama kali diisolasi dari ubur-ubur victoria Aequorea. GFP dari A. victoria memiliki puncak eksitasi besar pada panjang gelombang 395 nm dan satu kecil di 475 nm. Puncak emisi adalah pada 509 nm, yang di bagian bawah hijau dari spektrum sinar tampak.
Struktur Green Flourescent Protein (GFP)
GFP memiliki struktur beta barel khas, yang terdiri dari sebelas β-sheet dengan enam 𝛼 −heliks yang berisi kovalen kromofor 4-(p-hidroksibenzilIdena) imidazolidin-5-one (HBI). Prinsip fluorofor di GFP adalah adanya tripeptida yang terdiri atas residu serin, tirosin, dan glisin pada posisi 65-67. Walaupun motif asam amino ini sederhana dan umumnya ditemukan di seluruh alam, namun umumnya tidak menyebabkan fluoresensi. Hal ini dikarenakan adanya proses
Gambar 5. Struktur GFP modifikasi pasca-translasi dari asam amino penyusun GFP, membentuk kromofor, dimana jaringan ikatan hidrogen dan interaksi elektron-susun dengan rantai samping ini akan mempengaruhi warna, intensitas dan kestablian sinar GFP.
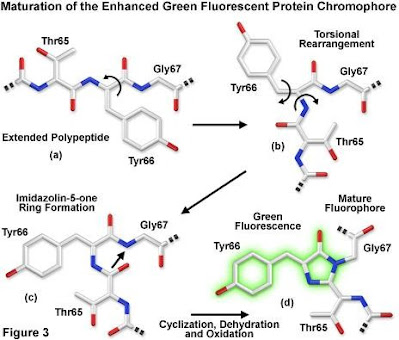
Proses modifikasi asam amino pembentuk GFP
Gambar diatas adalah diagram skematik dari pembentukan kromofor dari GFP, sebuah derivat menggantikan asam amino treonin dengan asam amino serin di posisi 65 (S65T). Pada Gambar 6 (a) , urutan pra - pematangan GFP fluorofor tripeptida asam amino (Thr65 - Tyr66 - Gly67 ) ditarik ke dalam konfigurasi yang lurus sehingga residu treonin diposisikan di sudut kiri atas diagram. Langkah pertama dalam urutan pematangan dianggap serangkaian penyesuaian ikatan peptida dan rantai samping torsi yang memindahkan karbon karboksil dari asam amino serin pada posisi 65 (Ser65) di dekat atom nitrogen amino dari residu glisin pada posisi 67 (Gly67). Serangan nukleofilik oleh atom karbon ini pada nitrogen amida glisin, diikuti oleh dehidrasi, sehingga menghasilkan imidazolin-5-one yaitu sistem cincin heterosiklik terkonjugasi. Fluoresensi terjadi ketika oksidasi ikatan alpha - beta karbon pada tirosin (Tyr66) oleh molekul oksigen memperlebar konjugasi elektron dari sistem cincin imidazolin untuk memasukkan cincin fenil tirosin dan yang substituen para-oksigen. Hasilnya, π - elektron pada sistem resonansi yang sangat terkonjugasi yang sebagian besar menyumbang sifat spektroskopi dari protein. Studi mutagenesis ekstensif menunjukkan bahwa residu glisin pada posisi 67 sangat penting dalam pembentukan kromofor, dan memang, tidak ada GFP yang tidak memiliki elemen penting ini.
Kegunaan Green Flourescent Protein (GFP)
Ketersediaan GFP dan turunannya telah benar-benar menguntungkan bagi ilmu tentang fluoresensi dan cara digunakan dalam biologi sel dan disiplin ilmu biologi lainnya. Sementara sebagian besar molekul neon kecil seperti FITC (fluorescein isothiocyanate) sangat phototoxic bila digunakan dalam sel hidup, protein fluorescent seperti GFP tidak memiliki efek racun jika diterangi dalam sel hidup. Hal in telah memicu perkembangan sangat pesat pada sistem mikroskopis fluoresensi - sel hidup , yang dapat digunakan untuk mengamati sel-sel dari waktu ke waktu mengungkapkan satu atau lebih protein dengan protein fluorescen. Sebagai contoh, GFP telah banyak digunakan dalam pelabelan spermatozoa dari berbagai organisme untuk keperluan identifikasi seperti pada Drosophila melanogaster (lalat buah), di mana ekspresi GFP dapat digunakan sebagai penanda untuk karakteristik tertentu. GFP juga dapat dinyatakan dalam struktur yang berbeda memungkinkan perbedaan morfologi. Dalam kasus tersebut, gen untuk produksi GFP disambung ke dalam genom organisme di wilayah DNA dengan kode untuk protein target dan yang dikendalikan oleh urutan asam amino yang sama, yaitu gen regulasi. Dalam sel tempat gen tersebut diekspresikan, protein yang telah ditandai diproduksi. Pada saat yang bersamaan GFP juga diproduksi. Dengan demikian, hanya sel-sel di mana gen tagged diungkapkan atau protein target yang diproduksi yang akan berpendar bila diamati di bawah mikroskop fluoresensi.
Semakin berkembang jaman, sekarang ini juga telah ditemukan bahwa GFP dapat disisipkan di berbagai jenis binatang, diantaranya yang sudah dilakukan adalah pada tikus, kelinci, kucing, monyet, dll. Dalam penelitian tentang GFP juga ditemukan bahwa tikus yang telah disisipi GFP transgenik dapat digunakan sebagai terapi gen serta pengobatan regeneratif.
Cara Membuat GloFish
Transgen yang diperkenalkan ke GloFish terdiri dari dua bagian. Bagian pertama adalah promotor dan bagian kedua adalah urutan coding untuk protein reporter. Promotor A mengontrol di mana dan kapan gen akan diekspresikan. Promotor GloFish adalah otot spesifik yang disebut mylz2 promotor . Sedangkan protein reporter digunakan untuk menandai sel. Transgen GloFish mengkodekan protein fluorescent reporter yang berasal dari ubur-ubur yang memiliki fluoresensi endogen. Sekarang ada banyak warna GloFish diantara Green Fluorescent Protein (GFP), Red Fluorescent Protein (RFP), Yellow Fluorescent Protein (YFP), Blue Fluorescent Protein (BFP), dan Purple Fluorescent Protein (PFP) (http://www. GloFish.com/). Promotor otot mylz2 begitu kuat sehingga ikan zebra ini akan berwarna cerah walaupun hanya berada di bawah cahaya putih normal.
Metode yang dikembangkan untuk penyisipan DNA ke dalam embrio ikan zebra diantaranya adalah injeksi, infeksi retroviral, penggunaan microprojectiles dan transfer gen dengan |media listrik. Injeksi DNA plasmid telah terbukti menjadi sarana yang dapat diandalkan dan tetap menjadi metode paling banyak yang digunakan untuk memproduksi ikan zebra transgenik. Dengan injeksi DNA, ikan zebra transgenik dihasilkan melalui penyuntikan plasmid superkoil dan linierisasi. Namun, DNA linier lebih mungkin diintegrasikan secara stabil ke dalam genom. Setelah injeksi, DNA plasmid linear umumnya disusun kembali menjadi kepala ke ekor konkatamer dan terintegrasi pada satu bagian. Pembelahan sel yang cepat dalam embrio ikan zebra menyokong integrasi DNA asing selama tahap akhir pembangunan, sehingga terlihatlah pola ekspresi mosaik pada ikan zebra tersebut.
DNA telanjang dapat mikroinjeksi ke dalam sitoplasma embrio ikan zebra pada tingkat 200/h. Sekitar 23% dari embrio ikan zebra yang telah diinjeksi ini dapatbertahan mencapai kematangan seksualnya. Gen yang akan disisipkan kemudian ditransmisikan ke antara 2 dan 50% dari generasi F1, namun generasi berikutnya menampilkan Mendel benar warisan (38,41). Rendahnya tingkat transmisi ke generasi F1 membatasi tingkat di mana ikan transgenik dapat dihasilkan. Namun, bila dikombinasikan dengan cara sederhana dan cepat mengidentifikasi transgenik, sistem ikan zebra menjadi sangat efisien.
Collas dan Aleström telah melaporkan injeksi sitoplasma DNA nuklir sinyal lokalisasi (NLS) kompleks dalam telur ikan zebra sebagai sarana meningkatkan penyerapan DNA oleh inti embrio. Penulis ini menunjukkan bahwa kompleks NLS dapat meningkatkan efisiensi transmisi germline. Transparansi embrio ikan zebra dapat dimanfaatkan dengan menggunakan GFP sebagai reporter untuk transformasi.
Meskipun konsepnya sederhana, namun gangguan spesifik dan manipulasi gen dalam organisme telah terbukti tugas yang sulit dan menuntut. Kurangnya sel induk embrional untuk ikan zebra, membutuhkan pendekatan radikal yang berbeda untuk mencapai penargetan gen organisme utuh tanpa gangguan. Dalam konteks ini, kemajuan signifikan telah dibuat selama 10 tahun terakhir dalam mengembangkan reagen sintetis yang mengenali dan mengikat target yang diinginkan di dsDNA. Dua reagen, helix-invading peptide nucleic acids (PNAs) and triplex-forming oligonucleotides (TFOs) ditemukan dan berpotensi menjadi inhibitor dari transkripsi, serta dapat digunakan untuk mutagenesis gen. Tindakan reagen ini berdasarkan pada penargetan dari DNA homopurine, sehingga membentuk struktur triple heliks. Struktur yang dapat menghambat transkripsi melalui halangan sterik dari transkripsi menawarkan alternatif kompleks untuk antisense dan RNA gangguan untuk ekspresi gen. Konsentrasi yang lebih rendah dari oligonukleotida akan diperlukan per sel untuk mengerahkan efek penargetan salinan kromosom gen, bukan salinan mRNA.
Dampak dari Adanya GloFish
Sejak Yorktown Teknologi pertama kali menjual ikan zebra yang telah mengalami modifikasi genetic menjadi hewan peliharaan yang dimodifikasi secara pada tahun 2003, GloFish, telah menjadi ikan akuarium yang populer, dengan jutaan ekor telah dijual dalam dalam berbagai warna. Selain menjadi peliharaan yang popular di Amerika Serikat, penjualan ikan ini juga menimbulkan pro dan kontra dari berbagai pihak. Center for Food Safety, pusat keamanan makanan Amerika Serikat memberikan gugatan untuk menghentikan penjualannya karena dinilai akan mencemari lingkungan dan berbahaya bagi kesehatan. Sementara itu, akademisi mulai berpikir tentang bagaimana menggunakan ini Danios berwarna cerah untuk mengajarkan tentang konsep-konsep dalam genetika , dari pewarisan Mendel statistik dan rekayasa genetika itu sendiri .
Pada bulan Februari 2012, Yorktown memperkenalkan GloFish dengan warna Hijau Tetra, yang merupakan ikan tetra hitam yang telah direkayasa genetikanya. Seperti sepupunya ikan zebra lainnya, GloFish jenis ini adalah ikan air tawar kecil yang mencakup materi genetik dari karang neon yang membuatnya neon terang. Di bawah cahaya hitam, bersinar dalam gelap.
Kedua GloFish ini sangat berbeda, namun ahli lingkungan dan beberapa ahli mengatakan bahwa hal ini sangat penting. Ikan zebra yang menyukai suhu panas adalah ikan dari Asia selatan dan tidak bisa bertahan lama di perairan Amerika Serikat yang dingin. Dengan demikian, Food and Drug Administration telah memutuskan bahwa akan ada sedikit ancaman invasi perairan AS jika ikan-ikan ini dipelihara di akuarium rumah. Di South Florida, ikan zebra dengan genetic tetra hitam dimodifikasi bisa mengganggu lingkungan. Di Amerika Selatan, mereka bisa berarti gangguan yang tidak diinginkan dalam keanekaragaman hayati.
Bukan tidak mungkin, pemelihara GloFish melepaskan ikannya ke perairan sehingga akan adanya persaingan antara ikan GloFish dan ikan asli dari daerah tersebut yang bisa melemahkan keturunan dari ikan asli sehingga akan mempengaruhi spesies ikan asli. GloFish dapat memberikan kerugian karena mereka mencari makanan atau dalam peran mereka sebagai mangsa dan pemangsa. Jika tetras GloFish berkembang biak dengan tetras hitam liar maka gen fluorescent akan diteruskan ke sejumlah generasi yang menyebabkan perubahan di alam. Ikan rekayasa genetika tidak diperbolehkan di Kanada dan sebagian besar Negara Eropa, dan GloFish tidak bisa dijual di California. FDA menetapkan pada tahun 2003 yang GloFish tidak perlu melalui proses persetujuan penuh, dengan mengatakan bahwa tidak ada bukti ikan yang diubah genetiknya menimbulkan peningkatan risiko terhadap lingkungan. Hingga saat ini, masih dilakukan penelitian tentang efek adanya GloFish bagi lingkungan sehingga belum pasti apakah GloFish berbahaya bagi lingkungan atau tidak.
Referensi
- Adam Amsterdam, d. (2000). The Aequorea victoria Green Flourescent Protein Can Be Used a Reporter in LIves Zebrafish Embryos.
- Andrew Dodd, d. (2000). Zebrafish: Bridging The Gap Between Development and Desease. Oxford Unibersity Press .
- Anonimous. (2013). GloFish. http://www.GloFish.com/
- Anonimous. Zebrafish. http://en.wikipedia.org/wiki/Zebrafish
- Campus, Z. (t.thn.). Introduction to Flouroscent Protein. http://zeiss-campus.magnet.fsu.edu
- Mogel, K. H. (2012, September 18). Are GloFish Bad for Environment. http://www.biofortified.org/
- Nash, S. (2004). Glofish Gives New Shine to GM Debate. www.nwrage.org



Tidak ada komentar:
Posting Komentar